Удельная теплоемкость воды калориях
Содержание статьи
Удельная теплоёмкость
Молекулы имеют внутреннюю структуру, образованную атомами, которые могут совершать колебания внутри молекул. Кинетическая энергия, запасённая в этих колебаниях, отвечает не только за температуру вещества, но и за его теплоёмкость
Уде́льная теплоёмкость — это отношение теплоёмкости к массе, теплоёмкость единичной массы вещества (разная для различных веществ); физическая величина, численно равная количеству теплоты, которое необходимо передать единичной массе данного вещества для того, чтобы его температура изменилась на единицу.[1].
В Международной системе единиц (СИ) удельная теплоёмкость измеряется в джоулях на килограмм на кельвин, Дж/(кг·К)[2]. Иногда используются и внесистемные единицы: калория/(кг·°C) и т. д.
Удельная теплоёмкость обычно обозначается буквами c или С, часто с индексами.
На значение удельной теплоёмкости влияет температура вещества и другие термодинамические параметры. К примеру, измерение удельной теплоёмкости воды даст разные результаты при 20 °C и 60 °C. Кроме того, удельная теплоёмкость зависит от того, каким образом позволено изменяться термодинамическим параметрам вещества (давлению, объёму и т. д.); например, удельная теплоёмкость при постоянном давлении (CP) и при постоянном объёме (CV), вообще говоря, различны.
Формула расчёта удельной теплоёмкости:
где
c — удельная теплоёмкость, Q — количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении), m — масса нагреваемого (охлаждающегося) вещества, ΔT — разность конечной и начальной температур вещества.
Удельная теплоёмкость зависит от температуры, поэтому более корректной является следующая формула с малыми (формально бесконечно малыми) и :
Значения удельной теплоёмкости некоторых веществ[править | править код]
Приведены значения удельной теплоёмкости при постоянном давлении (Cp).
Стандартные значения удельной теплоёмкости
| Вещество | Агрегатное состояние | Удельная теплоёмкость, кДж/(кг·K) |
|---|---|---|
| Водород | газ | 14,304[3] |
| Аммиак | газ | 4,359-5,475 |
| Гелий | газ | 5,193[3] |
| Вода (300 К, 27 °C) | жидкость | 4,1806[4] |
| Сусло пивное | жидкость | 3,927 |
| Литий | твёрдое тело | 3,582[3] |
| Этанол | жидкость | 2,438[5] |
| Лёд (273 К, 0 °C) | твёрдое тело | 2,11[6] |
| Водяной пар (373 К, 100 °C) | газ | 2,0784[4] |
| Нефтяные масла | жидкость | 1,670-2,010 |
| Бериллий | твёрдое тело | 1,825[3] |
| Азот | газ | 1,040[3] |
| Воздух (100 % влажность) | газ | 1,030 |
| Воздух (сухой, 300 К, 27 °C) | газ | 1,007[7] |
| Кислород (O2) | газ | 0,918[3] |
| Алюминий | твёрдое тело | 0,897[3] |
| Графит | твёрдое тело | 0,709[3] |
| Стекло кварцевое | твёрдое тело | 0,703 |
| Чугун | твёрдое тело | 0,554[8] |
| Алмаз | твёрдое тело | 0,502 |
| Сталь | твёрдое тело | 0,468[8] |
| Железо | твёрдое тело | 0,449[3] |
| Медь | твёрдое тело | 0,385[3] |
| Латунь | твёрдое тело | 0,920[8] |
| Молибден | твёрдое тело | 0,251[3] |
| Олово (белое) | твёрдое тело | 0,227[3] |
| Ртуть | жидкость | 0,140[3] |
| Вольфрам | твёрдое тело | 0,132[3] |
| Свинец | твёрдое тело | 0,130[3] |
| Золото | твёрдое тело | 0,129[3] |
| Значения приведены для стандартных условий (T = +25 °C, P = 100 кПа), если это не оговорено особо. | ||
Значения удельной теплоёмкости для некоторых строительных материалов
| Вещество | Удельная теплоёмкость кДж/(кг·K) |
|---|---|
| Древесина | 1,700 |
| Гипс | 1,090 |
| Асфальт | 0,920 |
| Талькохлорит | 0,980 |
| Бетон | 0,880 |
| Мрамор, слюда | 0,880 |
| Стекло оконное | 0,840 |
| Кирпич керамический красный | 0,840-0,880[9] |
| Кирпич силикатный | 0,750-0,840[9] |
| Песок | 0,835 |
| Почва | 0,800 |
| Гранит | 0,790 |
| Стекло кронглас | 0,670 |
| Стекло флинт | 0,503 |
| Сталь | 0,470 |
См. также[править | править код]
- Теплоёмкость
- Объёмная теплоёмкость
- Молярная теплоёмкость
- Теплоёмкость идеального газа
Примечания[править | править код]
- ↑ Для неоднородного (по химическому составу) образца удельная теплоемкость является дифференциальной характеристикой , меняющейся от точки к точке. Зависит она в принципе и от температуры (хотя во многих случаях изменяется достаточно слабо при достаточно больших изменениях температуры), при этом строго говоря определяется — вслед за теплоёмкостью — как дифференциальная величина и по температурной оси, то есть строго говоря следует рассматривать изменение температуры в определении удельной теплоёмкости не на один градус (тем более не на какую-то более крупную единицу температуры), а на малое с соответствующим количеством переданной теплоты . (См. далее основной текст.)
- ↑ Кельвины (К) здесь можно заменять на градусы Цельсия (°C), поскольку эти температурные шкалы (абсолютная и шкала Цельсия) отличаются друг от друга лишь начальной точкой, но не величиной единицы измерения.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — P. 4-135. — 2828 p. — ISBN 1420090844.
- ↑ 1 2 CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — P. 6-2. — 2828 p. — ISBN 1420090844.
- ↑ CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — P. 15-17. — 2828 p. — ISBN 1420090844.
- ↑ CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — P. 6-12. — 2828 p. — ISBN 1420090844.
- ↑ CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — P. 6-17. — 2828 p. — ISBN 1420090844.
- ↑ 1 2 3 Paul Evans. Specific heat capacity of materials (англ.). The Engineering Mindset (16 October 2016). Дата обращения: 14 июля 2019.
- ↑ 1 2 Плотность и удельная теплоемкость кирпича: таблица значений.
Литература[править | править код]
- Таблицы физических величин. Справочник, под ред. И. К. Кикоина, М., 1976.
- Сивухин Д. В. Общий курс физики. — Т. II. Термодинамика и молекулярная физика.
- Лифшиц E. М. Теплоёмкость // под. ред. А. М. Прохорова Физическая энциклопедия. — М.: «Советская энциклопедия», 1998. — Т. 2.
Источник
Удельная теплоёмкость
АльтИнфоЮг
Альтернативная энергетика и информация
ЗДОРОВЬЕ И ДЕНЬГИ ЗДЕСЬ
Чтоб вы все были здоровы и богаты долгие годы. ЖМИ!
Удельная теплоёмкость вещества означает количество теплоты, необходимое для нагрева единицы веществ на один градус. Чаще всего за единицу вещества берётся масса в 1 кг. Реже используются единицы объёма, например, кубометр или литр. В химии при термохимических реакциях используется молярная теплоёмкость, когда за единицу вещества принимают моль. Удельная теплоёмкость заметно меняется при изменении температуры и в большей степени при изменении агрегатного состояния вещества, например, значения теплоёмкости воды будут разными в жидком, твёрдом и газообразном состоянии. В приведённой таблице указывается также температура и агрегатное состояние вещества.
Удельная теплоёмкость материалов
| Наименование материала | Температура 0С | Удельная теплоёмкость | |
|---|---|---|---|
| кДж /(кг · К) | кал /(г · 0С) | ||
| Удельная теплоёмкость газов и паров | |||
| Азот | 0 — 200 | 1,0 | 0,25 |
| Водород | 0 — 200 | 14,2 | 3,41 |
| Водяной пар | 100 — 500 | 2,0 | 0,48 |
| Воздух | 0 — 400 | 1,0 | 0,24 |
| Гелий | 0 — 600 | 5,2 | 1,24 |
| Кислород | 20 — 440 | 0,92 | 0,22 |
| Оксид углерода | 26 — 200 | 1,0 | 0,24 |
| Пары спирта | 40 — 100 | 1,2 | 0,29 |
| Хлор | 13 — 200 | 0,5 | 0,12 |
| Удельная теплоёмкость жидкостей при нормальном атмосферном давлении | |||
| Бензин (Б-70) | 20 | 2,05 | 0,49 |
| Вода | 1 — 100 | 4,19 | 1,00 |
| Глицерин | 0 — 100 | 2,43 | 0,58 |
| Керосин | 0 — 100 | 2,09 | 0,50 |
| Масло машинное | 0 — 100 | 1,67 | 0,40 |
| Масло подсолнечное | 20 | 2,43 | 0,58 |
| Молоко | 20 | 3,94 | 0,94 |
| Нефть | 0 — 100 | 1,67 — 2,09 | 0,40 — 0,50 |
| Ртуть | 0 — 300 | 0,138 | 0,033 |
| Спирт | 20 | 2,47 | 0,59 |
| Эфир | 18 | 3,34 | 0,80 |
| Удельная теплоёмкость расплавленных металлов и сжиженных газов | |||
| Азот | -200,4 | 2,01 | 0,48 |
| Алюминий | 660 — 1000 | 1,09 | 0,36 |
| Водород | -257,4 | 7,41 | 1,77 |
| Воздух | -193,0 | 1,97 | 0,47 |
| Гелий | -269,0 | 4,19 | 1,00 |
| Золото | 1055 — 1300 | 0,14 | 0,034 |
| Кислород | -200,3 | 1,63 | 0,39 |
| Натрий | 100 | 1,34 | 0,33 |
| Олово | 250 | 0,25 | 0,060 |
| Свинец | 327 | 0,16 | 0,039 |
| Серебро | 960 — 1300 | 0,29 | 0,069 |
| Удельная теплоёмкость твёрдых веществ | |||
| Азот твёрдый | -250 | 0,46 | 0,11 |
| Бетон | 20 | 0,88 | 0,21 |
| Бумага | 20 | 1,50 | 0,36 |
| Воздух твёрдый | -193 | 2,00 | 0,47 |
| Графит | 0 — 100 | 0,75 | 0,18 |
| Дерево: | |||
| дуб | 0 — 100 | 2,40 | 0,57 |
| ель, сосна | 0 — 100 | 2,70 | 0,65 |
| Каменная соль | 0 — 100 | 0,92 | 0,22 |
| Камень | 0 — 100 | 0,84 | 0,20 |
| Кирпич | 0,88 | 0,21 | |
| Кислород твёрдый | -200,3 | 1,60 | 0,39 |
| Лёд | -40 — 0 | 2,10 | 0,50 |
| Нафталин | 20 | 1,30 | 0,31 |
| Парафин | 20 | 2,89 | 0,69 |
| Пробка | 0 — 100 | 2,00 | 0,48 |
| Стекло: | |||
| обыкновенное | 0 — 100 | 0,67 | 0,16 |
| зеркальное | 0 — 100 | 0,79 | 0,19 |
| лабораторное | 0 — 100 | 0,84 | 0,20 |
| Фарфор | 0 — 100 | 1,10 | 0,26 |
| Шифер | 20 | 0,75 | 0,18 |
| Удельная теплоёмкость металлов и сплавов | |||
| Алюминий | 0 — 200 | 0,92 | 0,22 |
| Вольфрам | 0 — 1000 | 0,15 | 0,035 |
| Железо | 0 — 500 | 0,54 | 0,13 |
| Золото | 0 — 500 | 0,13 | 0,032 |
| Иридий | 0 — 1000 | 0,15 | 0,037 |
| Магний | 0 — 500 | 1,10 | 0,27 |
| Медь | 0 — 500 | 0,40 | 0,097 |
| Никель | 0 — 300 | 0,50 | 0,12 |
| Олово | 0 — 200 | 0,23 | 0,056 |
| Платина | 0 — 500 | 0,14 | 0,033 |
| Свинец | 0 — 300 | 0,14 | 0,033 |
| Серебро | 0 — 500 | 0,25 | 0,059 |
| Сталь | 50 — 300 | 0,50 | 0,12 |
| Цинк | 0 — 300 | 0,40 | 0,097 |
| Чугун | 0 — 200 | 0,54 | 0,13 |
Соотношение между единицами удельной теплоёмкости
| Единицы удельной теплоёмкости | Дж /(кг · К) | кДж/ (кг · К) | кал /(г · 0С) или ккал/(кг · 0С) |
|---|---|---|---|
| 1 Дж /(кг · К) | 1 | 0,001 | 2,39 · 10-4 |
| 1 кДж/ (кг · К) | 1000 | 1 | 0,239 |
| 1 кал /(г · 0С) = 1 ккал/(кг · 0С) | 4,19 · 103 | 4,19 | 1 |
| Примечание: 1 кал /(г · 0С) = 1 ккал/(кг · 0С) = 4186,8 Дж /(кг · К) = 4,1868 кДж /(кг · К). Градусы по Цельсию и Кельвину равны по модулю. | |||
Значения удельной теплоёмкости и соотношения между единицами измерений даны по книге «Справочник по физике и технике» А.С. Енохович.
Источник
Удельная теплоемкость воды
Удельная теплоемкость — это физическая величина, которая используется для расчета количества теплоты, необходимого для нагревания вещества до определенной температуры. При понижении температуры значение этой величины применяется для оценки количества теплоты, которое выделится в процессе охлаждения, а удельные теплоемкости различных веществ могут иметь значения, отличающиеся в десятки раз. Повседневная жизнь человека в значительной степени зависит от качества воды и ее параметров, в ряду которых удельная теплоемкость воды занимает важное место.

Общее определение удельной теплоемкости
Напомним, что передача энергии от одного тела к другому без совершения работы называется теплопередачей или теплообменом. Теплообмен происходит, когда тела имеют разные температуры. Величина энергии, переданная телу в результате теплообмена, называется количеством теплоты Q. В соответствии с первым законом термодинамики количество теплоты Q равно изменению внутренней энергии тела ΔU:
$ Q = ΔU $ (1).
Следует помнить, что количество теплоты определяет только изменение внутренней энергии, а не его конкретное значение. Полная величина внутренней энергии — это сумма потенциальной энергии взаимодействия частиц, из которых состоит физическое тело, и кинетической энергии их беспорядочного движения.

Рис. 1. Что такое теплообмен и теплопередача
Изменение внутренней энергии пропорционально массе тела m и изменению температуры:
$ Q = ΔU = c*m* ΔT $ (2),
где: $ΔT = T_k — T_н$ -разница между конечной и начальной температурами.
Коэффициент пропорциональности c в формуле (2) называется удельной теплоемкостью вещества:
$ c = {Qover m* ΔT} $ (3).
В Международной системе СИ количество теплоты измеряется в джоулях, масса — в килограммах, а разница температур — в градусах Кельвина. Значит единица измерения удельной теплоемкости будет:
$ [c] ={ [1 Дж]over [1 кг]*[1^0 K] } $ (4).
Из формул (3), (4) следует, что величина удельной теплоемкости показывает, какое количество теплоты необходимо, чтобы нагреть 1 кг вещества на 10K.
Раньше, до принятия в системе СИ в качестве единицы измерения энергии джоуля, использовалась специальная единица — калория (кал), равная количеству теплоты, которое нагревает 1 грамм воды на 1 градус Цельсия. Опытным путем определен, так называемый, механический эквивалент теплоты — соотношение между джоулем и калорией:
$ 1 кал = 4,2 Дж $
В настоящее время данную единицу используют при определении количества потребленной тепловой энергии в жилых домах и на предприятиях.
Значения удельных теплоемкостей для твердых, жидких и газообразных веществ определены с помощью физических измерений и сведены в справочные таблицы.
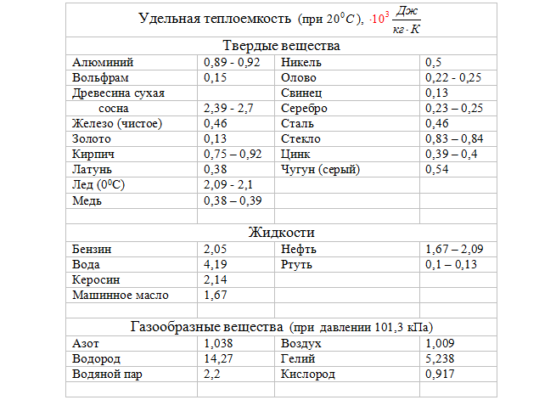
Рис. 2. Таблица значений удельной теплоемкости
Особенности удельной теплоемкости воды
Из приведенной таблицы видно, что у металлов значения теплоемкостей довольно низкие (например у свинца это 140 Дж/кг*0K), поэтому для нагрева металлических предметов требуются немного тепла. Удельная теплоемкость воды равна 4200 Дж/кг*0K, что на много больше аналогичных металлических параметров. Исследования показали, что это одно из самых высоких значений среди жидких материалов.
В твердом агрегатном состоянии вода (лед) имеет в два раза меньшее значение удельной теплоемкости — 2100 Дж/кг*0K, а в газообразном состоянии (водяной пар) — 2200 Дж/кг*0K.
Табличные значения для удельных теплоемкостей приводятся, как правило, для фиксированных температур в диапазоне 20-250С (нормальная или комнатная температура). Это связано с тем, что величина удельной теплоемкости зависит от температуры, что характерно не только для воды, но и для других веществ. На приведенном ниже графике показана экспериментально полученная зависимость удельной теплоемкости воды при различных температурах. Видно, что 00С до 370С теплоемкость воды снижается, а затем снова растет. Точное определение удельной теплоемкости воды производится с помощью приборов, называемых калориметрами.
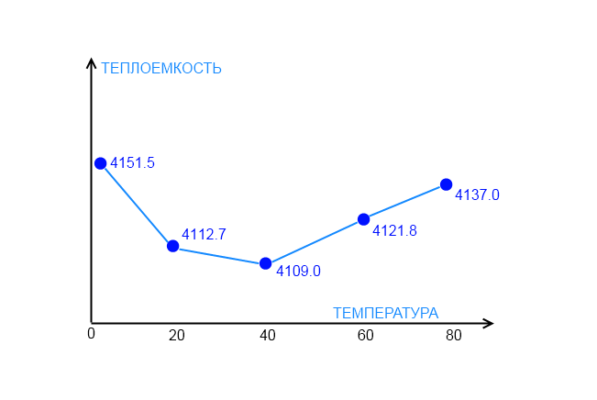
Рис. 3. График зависимости удельной теплоемкости воды от температуры
Обладание водой максимальной величиной удельной теплоемкости приводит к следующим полезным применениям в различных сферах человеческой деятельности:
- Использование воды в отопительных системах домов в качестве теплоносителя, который долго сохраняет тепло;
- Охлаждение водой металлических деталей, которые нагреваются в процессе механической обработки;
- Вода является одним из самых эффективных средств пожаротушения. Во время контакта с пламенем она превращаясь пар, отнимает большое количество теплоты у горящих материалов;
- Скорость тушения пламени дополнительно повышает водяной пар, который обволакивая горящий предмет, препятствует поступлению кислорода, без которого горение прекращается. Кстати, огонь эффективнее тушить горячей водой, так как у горячей воды образование пара произойдет быстрее;
- В районах проживания, расположенных рядом с большими водоемами (морем или океаном) летом не бывает слишком жарко, а зимы не очень холодные. В течение лета вода, нагреваясь, накапливает большое количество тепла. А зимой происходит медленное (из-за большой теплоемкости) остывание, что и является причиной мягкого зимнего климата приморских городов.
Что мы узнали?
Итак, мы узнали, что величина удельной теплоемкости показывает, какое количество теплоты необходимо, чтобы нагреть 1 кг вещества на 10K. Значение удельной теплоемкости воды равно 4200 Дж/кг*0K при нормальных температурах. Имеется температурная зависимость теплоемкости воды от температуры. Точные значения этой величины получены экспериментально и приведены в справочниках в виде таблиц и графиков.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
-
Айана Капсаргина
5/5
Оценка доклада
Средняя оценка: 4.3. Всего получено оценок: 139.
Источник
Удельная теплоемкость воды, газов, паров и различных веществ (Таблица)
Удельная теплоёмкость (с) — это физическая величина, равная численно количеству теплоты, которое необходимо передать единице массе данного вещества для того, чтобы его температура изменилась на единицу.
В системе единиц (СИ) удельная теплоёмкость обозначается в джоулях на килограмм на кельвин, Дж/(кг·К).
Удельная теплоемкость расчитывается по следующей формуле:
где Q — количество теплоты, полученное веществом при нагревании,
m — масса нагреваемого или охлаждаемого вещества,
ΔT — разность конечной и начальной температур вещества.
Удельная теплоемкость воды
Международный Комитет Мер и Весов принял в 1950 г. предложенные В. Дж. де Хаасом значения: cv = (15° С) = 4,1855дж/г · град С (соответствует значению, данному Бэрджем в 1941 г.); отсюда для ср(t °C) получается следующая формула:
Эта формула была дана Осборном, Стимсоном и Гиннингсом.
Во всех последующих таблицах значения с даны в единицах дж/г · град · С
Температура, °С | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | |
4,2174 | 4,2138 | 4,2104 | 4,2074 | 4,2045 | 4,2019 | 4,1996 | 4,1974 | 4,1954 | 4,1936 | |
10 | 4,1919 | 4,1904 | 4,1890 | 4,1877 | 4,1866 | 4,1855 | 4,1846 | 4,1837 | 4,1829 | 4,1822 |
20 | 4,1816 | 4,1810 | 4,1805 | 4,1801 | 4,1797 | 4,1793 | 4,1790 | 4,1787 | 4,1785 | 4,1783 |
30 | 4,1782 | 4,1781 | 4,1780 | 4,1780 | 4,1779 | 4,1779 | 4,1780 | 4,1780 | 4,1781 | 4,1782 |
40 | 4,1783 | 4,1784 | 4,1786 | 4,1788 | 4,1789 | 4,1792 | 4,1794 | 4,1796 | 4,1799 | 4,1801 |
50 | 4,1804 | 4,1807 | 4,1811 | 4,1814 | 4,1817 | 4,1821 | 4,1825 | 4,1829 | 4,1833 | 4,1837 |
60 | 4,1841 | 4,1846 | 4,1850 | 4,1855 | 4,1860 | 4,1865 | 4,1871 | 4,1876 | 4,1882 | 4,1887 |
70 | 4,1893 | 4,1899 | 4,1905 | 4,1912 | 4,1918 | 4,1925 | 4,1932 | 4,1939 | 4,1946 | 4,1954 |
80 | 4,1961 | 4,1969 | 4,1977 | 4,1985 | 4,1994 | 4,2002 | 4,2011 | 4,2020 | 4,2029 | 4,2039 |
90 | 4,2048 | 4,2058 | 4,2068 | 4,2078 | 4,2089 | 4,2100 | 4,2111 | 4,2122 | 4,2133 | 4,2145 |
Удельная теплоемкость тяжелой воды
Даны значения по отношению к обычной воде (ср — 1,000 при 20° С).
Температура, °С | 10 | 20 | 30 | 40 | 50 |
Удельная теплоемкость | 1,0097 | 1,0063 | | 1,0044 | 1,0037 | 1.0041 |
Удельная теплоемкость ртути
Ртуть имеет минимум удельной теплоемкости при 140° С.
Температура, °С | 20 | 40 | 60 | 80 | 100 | 200 | |
Удельная теплоемкость ртути | 0,1402 | 0,1394 | 0,1385 | 0,1377 | 0,1373 | (0,137) | (0,134) |
Удельная теплоемкость газов и паров (таблица)
Значения при постоянном давлении относятся обычно к атмосферному давлению.
Газ | Температура | Удельная теплоемкость |
При постоянном объеме (сp) | ||
Азот 1) | 0,732 | |
Аргон | 0-2 000 | 0,3122 |
Водород 2) | ок. 50 | 10,05 |
Воздух 3) | 0,718 | |
Окись углерода СО | 1000 | 0,950 |
Окись углерода СО | 1800 | 1,002 |
Пары воды | 100 | 1,463 |
Углекислый газ 4) | ок. 55 | 0,691 |
При постоянном давление (cv) | ||
Азота закись N3O | 26-103 | 0,892 |
Азота окись NO | 13-171 | 0,971 |
Азота перекись NO2 | 27-67 | 0,680 |
Аргон | 15 | 0,523 |
Воздух (сухой) | 20 | 1,006 |
Воздух (сухой) | 100 | 1,011 |
Воздух (сухой) | 500 | 1,092 |
Воздух (сухой) | 1000 | 1,192 |
Воздух (сухой) | -100 | 1,008 |
Воздух (сухой) (100 атм) | -80 | 1,902 |
Сероуглерод CS2 | 86-190 | 0,670 |
Скипидар C10h2 | 179-249 | 2,118 |
Спирт метиловый СН2O | 101-223 | 1,917 |
Хлороформ СНСl3 | 27-118 | 0,603 |
Эфир этиловый (C2H5)2O | 25-111 | 1,791 |
1) Для N сv = 0,732 + 0,00067t, t обозначает температуру. 2) Для Н cv уменьшается с увеличением плотности и понижением температуры. 3) Для воздуха cv = 0,7184 + 0,1167р, где р обозначает плотность (г/мл). 4) Для СО2, cv= 0,691 + 0,889Р + 1,42р2. | ||
Удельные теплоемкости различных веществ — жидкости, сплавы (таблица)
В большинстве случаев значения удельных теплоемкостей, данные в таблице, следует рассматривать как средние приближенные величины.
Вещество | Температура, C | Удельная теплоемкость |
Различные вещества | ||
Асбест | 20-100 | 0,84 |
Базальт | 20-200 | 0,84-1,00 |
Гранит | 20-100 | 0,80-0,84 |
Кварц SiO2 | 0,73 | |
Кварц SiO2 | 350 | 1,17 |
Кремнезем (плавленый) | 15-200 | 0,84 |
Кремнезем (плавленый) | 15-800 | 1,04 |
Лед | -250 | 0,15 |
| Лед | -160 | 1,0 |
| Лед | -21-1 | 2,0-2,1 |
Мрамор белый | 18 | 0,88-0,92 |
Парафин | 0-20 | 2,9 |
Песок | 20-100 | 0,80 |
Плавиковый шпат СаF2 | 30 | 0,88 |
Резина | 15-100 | 1,13-2,1 |
Стекло иенское 16»’ | 18 | 0,80 |
Стекло иенское 59»’ | 18 | 0,80 |
Стекло крон | 10-50 | 0,67 |
Стекло пирекс | 26 | 0,78 |
Стекло флинт | 10-50 | 0,50 |
Фарфор | 15-1000 | 1,07 |
| Фарфор | 15-200 | 0,75 |
Эбонит | 20-100 | 1,38 |
КСl | -250 | 0,0653 |
КСl | -187 | 0,490 |
КСl | 277 | 0,741 |
NaCl | -248 | 0,0414 |
NaCl | -38 | 0,825 |
NaCl | + 10 | 0,88 |
Сплавы | ||
Латунь желтая | 0,368 | |
Латунь красная (томпак) | 0,377 | |
Константан (эврика) | 18 | 0,410 |
Мягкий припой 1) | — | 0,176 |
Нейзильбер | 0-100 | 0,398 |
Жидкости | ||
Анилин | 15 | 2,15 |
Бензол | 10 | 1,42 |
Бензол | 40 | 1,77 |
Вода морская | 17 | 3,93 |
Глицерин | 18-50 | 2,43 |
Масло касторовое | 20 | 2,13 |
Масло льняное | 20 | 1,84 |
Масло парафиновое | 20-60 | 2,13- 2,26 |
Масло прованское | 7 | 1,97 |
Масло сурепное | 20 | 2,04 |
Рапа | -20 | 2,89 |
Рапа | 2,97 | |
Рапа | 15 | 3,01 |
Скипидар | 18 | 1,76 |
Спермацет | 20 | 2,06 |
Спирт амиловый | 18 | 2,30 |
Спирт метиловый | 12 | 2,52 |
Спирт этиловый | 2,29 | |
Спирт этиловый | 40 | 2,71 |
Толуол | 18 | 1,67 |
Эфир этиловый | 18 | 2,34 |
1) Sn 54%, Pb 46%; удельная теплоемкость = 0,1766 + 0,000159t; | ||
Отношение удельных теплоемкостей Cp и Cv для газов и паров
γ — отношение удельной теплоемкости при постоянном давлении к удельной теплоемкости при постоянном объеме.
Для непосредственного определения γ обычно применяется метод, основанный на адиабатическом расширении газа; для этого можно, например, определять скорость звука в газах. Зная давление или температуру непосредственно после адиабатического расширения (метод Клемана и Дезорма и метод Луммера и Прингсхейма), y можно найти из уравнений:
или
Газ | Температура, C | γ |
Одноатомные газы | ||
Аргон | 1,667 | |
Гелий | 1,63 | |
Криптон | 19 | 1,689 |
Ксенон | 19 | 1,666 |
Неон | 19 | 1,642 |
Пары ртути | 310 | 1,666 |
Двухатомные газы | ||
Азот | 20 | 1,401 |
Азота окись | — | 1,394 |
Водород | 4-17 | 1,407/8 |
Кислород | 5-14 | 1,400 |
Окись углерода | 1800 | 1,297 |
Воздух (сухой) | -79,3 | 1,405 |
Воздух (сухой) | 0-17 | 1,401/2 |
Воздух (сухой) | 500 | 1,357 |
Воздух (сухой) | 900 | 1,32 |
Воздух (сухой) (200 атм) | -79,3 | 1,828 2,333 |
Трехатомные газы | ||
Азота закись N2O | — | 1,324 |
Азота перекись N2O4 | 20 | 1,172 |
Азота перекись NO2 | 150 | 1,31 |
Аммиак NH3 | — | 1,336 |
Озон | — | 1,29 1) |
Пары воды | 100 | 1,334 |
Сернистый газ | 16-34 | 1,26 |
Сернистый газ | 500 | 1,2 |
Сероводород H2S | — | 1,340 |
Сероуглерод CS2 | — | 1,239 |
Углекислый газ | 4-11 | 1,300 |
Углекислый газ | 300 | 1,22 |
Углекислый газ | 500 | 1,20 |
Многоатомные газы | ||
Ацетилен С2Н2 | — | 1,26 |
Бензол | 20 | 1,40 |
Бензол | 99,7 | 1,105 |
Метан СН4 | — | 1,313- |
Метил бромистый | — | 1,274 |
Метил йодистый | — | 1,286 |
Метил хлористый | 19-30 | 1,279 |
Пропан С3Н8 | — | 1,130 |
Спирт метиловый | 99,7 | 1,256 |
Спирт этиловый | 53 | 1,133 |
Спирт этиловый | 99,8 | 1,134 |
Уксусная кислота | 136,5 | 1,147 |
Хлороформ СНСl3 | 24-42 99,8 | 1,110 1,150 |
Четыреххлористый углерод СС1 | — | 1,130 |
Этан С2Н6 | — | 1,22 |
Этил бромистый | — | 1,188 |
Этил хлористый | 22,7 | 1,187 |
Этилен С2Н4 | — | 1,264 |
Эфир этиловый | 12-20 | 1,024 |
Эфир этиловый | 99,7 | 1,112 |
1) Экстраполировано | ||
_______________
Источник информации: КРАТКИЙ ФИЗИКО-ТЕХНИЧЕСКИЙ СПРАВОЧНИК/ Том 1, — М.: 1960.
Источник