Артериальная гипертензия лишний вес
Содержание статьи
Как связаны гипертония и ожирение
Существует стереотип, что все люди с лишним весом — гипертоники. Большинство пациентов уверены, что ожирение и гипертония неразрывно связаны между собой и присутствие лишних килограммов обязательно несет гипертоническую болезнь. В некоторой степени это правда — гипертония и ожирение взаимосвязаны, но не всегда диагностируются вместе. Доктор Александр Юрьевич Шишонин, кандидат медицинских наук и автор эффективных лечебных методик по борьбе с нарушениями сердечно-сосудистой системы, объясняет, почему гипертоники могут быть худыми, а полные люди — иметь нормальное давление.
Что возникает раньше — гипертония или ожирение
Когда к доктору Шишонину приходят пациенты с лишним весом и повышенным артериальным давлением, Александр Юрьевич категорически запрещает садиться на диеты. Среди пациентов бытует миф, что быстрое похудение через диеты нормализует состояние кровеносных сосудов и сердца. Чтобы понять весь патогенетический механизм, врач предлагает ознакомиться с развитием гипертонии с медицинской точки зрения.
Представим череп, из которого идут шейные позвонки с боковыми отростками. В головном мозге имеется базальный отдел с тромбовидной ямкой. Она является центром регулирования артериального давления, частоты сокращений сердца и тонуса кровеносных сосудов. Из шейных позвонков по капиллярам и каронарам, находящимся в отростках, поступает кровь в ствол головного мозга и тромбовидную ямку. Таким способом кровь доставляет кислород и энергетические ресурсы в организм.
Когда кровоток нарушается по различным причинам, возникает компрессия позвоночных артерий, которые сдавливаются и не пропускают достаточное количество кислорода в мозг. Результатом компрессии становится:
- Кислородное голодание;
- Учащение пульса;
- Повышение артериального давления крови;
- Спазмы кровеносных сосудов;
- Гипертрофия сердечной мышцы.
Так развивается гипертония. Причинами сдавливания стенок капилляров могут быть:
- Гиподинамия — недостаток физической активности;
- Гипердинамия — переизбыток физических нагрузок;
- Психоэмоциональные расстройства;
- Злоупотребление алкоголем, табаком;
- Чрезмерное употребление соли, сахара, кофеина.
Что же происходит во время развития гипертонического синдрома? Мозг, ограниченный в поступлении кислорода, лишается энергетической подпитки. Чтобы восполнить ресурсы и силы для нормальной жизнедеятельности, мозговые рецепторы подают сигналы всем внутренним органам об увеличении выработки питательных веществ. Такими веществами являются глюкоза и углеводы.
Отсутствие кислорода требует большого количества углеводов и глюкозы, которые не успевают вырабатываться организмом. Рецепторы уже подают новые импульсы, и у пациента появляется тяга к сладкой и сытной пище, так как энергия поглощается голодным мозгом. Усиление аппетита приводит к ожирению. Тяга развивается к глюкозосодержащим и углеводосодержащим продуктам:
- сладости, мед, сахар;
- хлеб и мучные изделия;
- бобовые, злаки;
- картофель;
- кукуруза;
- яблоки, виноград, сухофрукты.
Также возникает постоянное чувство голода, которое человек пытается устранить, употребляя жирную или соленую пищу, фастфуд, газированные напитки. Регулярное употребление такой еды гарантированно обеспечивает лишним весом, поэтому гипертония и ожирение тесно связаны между собой.
Присоединяйтесь к Клубу Бывших Гипертоников, скачивайте гимнастику, которая помогла уже сотням тысяч человек победить скачки давления и гипертонию. Получайте самую актуальную и правильную информацию о проблемах, связанных с артериальным давлением, остеохондрозом, атеросклерозом, задавайте свои вопросы доктору Шишонину и просто общайтесь.
Помогают ли диеты при ожирении и артериальной гипертонии
Самое большое и ошибочное заблуждение людей с ожирением при гипертонии — это похудение с помощью диет и дальнейшее снижение давления. Любая диета становится огромным стрессом для организма, а нервные потрясения неприемлемы при лечении гипертонии. Ожирение — не повод голодать. Отказывая себе во многих продуктах, гипертоник по-прежнему ограничивает головной мозг в поступлении кислорода. Это влечет за собой закупоривание артерий, непроходимость крови и высокое артериальное давление.
Строгая диета при ожирении и гипертонии становится причиной астено-невротического вегетативного психоза, который грозит серьезными последствиями:
- Расстройства нервной системы;
- Нарушения пищеварения и ЖКТ;
- Проблемы с обменом веществ, почками;
- Сбой работы надпочечников;
- Гормональная дисфункция;
- Нарушения эндокринной системы.
Чтобы избавиться от ожирения при гипертонии, необходимо сначала наладить кровоток, после чего принимать меры по регулированию веса. Восстановить функции кровеносных артерий можно без медицинских препаратов, если следовать простым рекомендациям доктора Шишонина:
- Старайтесь меньше нервничать, настраиваться на позитив, окружить себя приятными людьми, увлечениями.
- Регулярно делайте дыхательную гимнастику и разминку шейного отдела позвоночника. Правильное дыхание позволяет увеличить приток воздуха, а разминка шеи уберет отечность, которая мешает нормальному кровотоку.
- Занимайтесь физическими нагрузками, больше ходите пешком. Не переусердствуйте, достаточно уделять зарядке 20-30 минут в день. Отлично подходят бег, прыжки, приседания, отжимания.
- Для профилактики пейте не препараты от гипертонии, а натуральные травяные настои и отвары. Нормализовать давление и улучшить работу кровеносной системы помогут чабрец, зверобой, пустырник, валерьянка.
Гипертония и ожирение тесно взаимосвязаны, но не стоит исключать гипертонический синдром у худых людей или приписывать его полным. Точный диагноз может поставить только квалифицированный врач-кардиолог после диагностических анализов.
Источник
Лечение ожирения – шаг к контролю артериального давления
Ожирение на сегодняшний день рассматривается как мировая эпидемия и одна из основных проблем общественного здравоохранения. В 2008 г. около 1,5 млрд взрослых людей во всем мире имели избыточный вес, 500 млн страдали ожирением. Во всем мире распространенность ожирения неуклонно растет на протяжении нескольких последних 10-летий: индекс массы тела (ИМТ) увеличивался на 0,4-0,5 кг/м2 во всем мире с 1980 по 2008 г. [1]. Ожирение ассоциировано с повышенной заболеваемостью, инвалидизацией и преждевременной смертностью от сердечно-сосудистых заболеваний (ССЗ), сахарного диабета (СД), рака и заболеваний опорно-двигательного аппарата. В зависимости от тяжести ожирения продолжительность жизни пациентов с избыточным весом и ожирением сокращается на срок от 4 до 10 лет [2-4], повышение смертности среди пациентов обусловлено в основном частым развитием ССЗ.
Артериальная гипертензия (АГ) наблюдается у большинства пациентов с ожирением — примерно у 80% мужчин и около 60% женщин, ее распространенность коррелирует со степенью ожирения и значительно повышает риск развития инсульта, инфаркта и заболеваний периферических артерий [5].
В этой связи наиболее актуальны обсуждение проблем, связанных с патогенезом развития АГ у пациентов с ожирением, и поиск способов коррекции массы тела и контроля уровня АД.
Патофизиологические механизмы развития АГ у пациентов с ожирением
Во многих исследованиях показано, что ожирение тесно коррелирует с АД и считается одним из ведущих факторов риска развития АГ [6, 7]. У тучных пациентов риск развития АГ в 2-3 раза превышает таковой у пациентов с нормальной массой тела [8]. Средние показатели систолического (САД) и диастолического (ДАД) АД у пациентов с ожирением превышают показатели АД у пациентов c нормальной массой тела на 9 и 7 мм рт. ст. у мужчин и на 11 и 6 мм рт. ст. — у женщин [9]. Даже у детей наличие ожирения, согласно канадским наблюдениям, в 7 раз повышает риск развития АГ [10].
Отличительной чертой первичного ожирения является чрезмерное отложение жира в организме. Первичное ожирение является следствием нарушения взаимодействий адипоцитов и гипоталамуса, по этой причине изменяется пищевое поведение больного; кроме того, дополнительное снижение физической активности усугубляет проблему. Многими авторами первичное ожирение характеризуется как алиментарно-конституционально-гиподинамическое. Главная отличительная черта первичного ожирения — это относительная (80%) или абсолютная (20%) лептинорезистентность с гиперлептинемией и, часто, гиперинсулинемией.
Жировая ткань состоит из зрелых адипоцитов, преадипоцитов, эндотелиальных клеток и макрофагов и на сегодняшний день рассматривается не как пассивное хранилище триглицеридов, а как самостоятельный эндокринный и паракринный орган [11, 12]. Адипоциты — функциональные единицы жировой ткани, способные синтезировать и секретировать в кровоток различные биологически активные соединения пептидной и непептидной природы. Избыток висцеральной жировой ткани у пациентов с избыточной массой тела и ожирением характеризуется гипертрофией адипоцитов и инфильтрацией ткани макрофагами.
Ожирение, связанное с АГ, некоторыми экспертами признается как отдельный фенотип, требующий тщательного подхода к диагностике, лечению и профилактике.
Ведущими механизмами развития АГ при ожирении являются активация симпатоадреналовой (САС) и ренин-ангиотензин-альдостероновой (РААС) систем [13].
Нейрогенный характер АГ при ожирении подтверждается повышением активности симпатической нервной системы (СНС) в сосудах почек и скелетной мускулатуры [14]. В исследовании NAS (Normotensive Aging Study) было обнаружено повышение уровня норадреналина в моче, пропорциональное ИМТ [15]. При снижении веса активность СНС уменьшается [16, 17]. Выраженное влияние на АД оказывают вегетативный дисбаланс и психоэмоциональный стресс, что проявляется в нарушении циркадного профиля, преимущественно САД. Чем больше вес, тем больше выражены колебания САД. У 50% пациентов с инсулинорезистентностью (ИР) наблюдаются симпатико- и гиперсимпатикотония. Гиперсимпатикотонический вариант функционирования сердечно-сосудистой системы ассоциируется с высокой степенью ожирения [18].
Возникновение АГ при ожирении связывают с ростом активности центральных отделов регуляции СНС под воздействием гиперинсулинемии и ИР. Инсулин может повышать активность САС сам по себе, но отчасти это может быть связано с действием лептина. Известно, что по мере увеличения степени ожирения тощаковый уровень лептина, который секретируется адипоцитами, растет. Лептин увеличивает активность СНС, особенно в почках. Это приводит, с одной стороны, к высокому выбросу и увеличению частоты сердечных сокращений, а с другой — к повышению реабсорбции натрия и увеличению внутрисосудистого объема крови [19].
Установлено наличие взаимосвязи между РААС и CНC. С активацией СНС связывают усиление секреции ренина в почках, и происходит это независимо от внутрипочечной сенсорной системы, регулирующей секрецию ренина почками. Более того, увеличение циклического аденозинмонофосфата под влиянием катехоламинов стимулирует экспрессию ангиотензиногена (АТ) в адипоцитах человека [20]. Таким образом, нарушение регуляции САС при ожирении также способно стимулировать активность РААС.
Гиперактивация РААС — один из ключевых механизмов развития АГ при ожирении. Исследования на животных показывают, что жировая ткань является дополнительным важным источником АТ, ангиотензинпревращающего фермента и ренина, и при наличии ожирения доля компонентов РААС, вырабатывающихся в жировой ткани, среди циркулирующих уровней этих компонентов становится весьма значимой [21].
Активность тканевой РААС тесно связана с продукцией адипокинов жировой тканью. Показано, например, что АТ II вызывает экспрессию лептина в адипоцитах [22]. Было высказано предположение, что такая активность свойственна только локально синтезируемому АТ II в отличие от системного АТ II [23].
Широко известно, что висцеральная жировая ткань вырабатывает большое количество биологически активных пептидов, многие из которых оказывают негативное влияние на развитие и прогрессирование АГ.
Самый известный гормон жировой ткани — лептин, он участвует в регуляции аппетита, активируя центр насыщения. Циркулирующие уровни лептина коррелируют с наличием и степенью ожирения и повышены у тучных людей. Оказывается, что у пациентов с избыточной массой тела развивается резистентность к лептину, и, несмотря на его высокую концентрацию в плазме, аппетит не подавляется.
Была обнаружена взаимосвязь между уровнем лептина и развитием АГ. Научные данные свидетельствуют о нескольких механизмах развития АГ при повышении уровня лептина. Во-первых, лептин изменяет активность почечной Na-, K-АТФ-азы, которая отвечает за уровень натрия [24]. Во-вторых, лептин активирует РААС. Также выявлена способность ренина к повышению активности СНС. Симпатическая стимуляция локальной почечной РААС, в свою очередь, ведет к повышению секреции АТ II, альдостерона, задержке воды и натрия в организме и, как следствие, к повышению АД. Дополнительный вклад в развитие АГ, опосредованной лептином, заключается в его способности к потенцированию прессорного эффекта норадреналина [25]. В-третьих, высокие уровни лептина связаны с резистентностью к инсулину, что тоже может быть одним из механизмов развития и прогрессирования гипертензии [26]. И, наконец, лептин может совместно с другими провоспалительными цитокинами вызывать внутрисосудистый окислительный стресс, что приводит к усугублению АГ [27].
Ведутся активный научный поиск молекулярных механизмов биосинтеза адипопродуцируемых гормонов, определение их роли в развитии ожирения, ИР и связанных с ними кардиоваскулярных заболеваний. Выявлено, что избыток висцеральной жировой клетчатки приводит к увеличению содержания гормонов, усиливающих проявление ИР (резистин, фактор некроза опухолей-α (ФНО-α), ингибитор активатора плазминогена-1 (ИАП-1), интерлейкин-6 (ИЛ-6), лептин, инсулиноподобный фактор роста-1), и снижению концентрации адипонектина, уменьшающего проявления ИР [28].

В дополнение к эффектам лептина гиперпродукция провоспалительных адипокинов ИЛ-6, ФНО-α, ИАП-1 и С-реактивного белка способствует развитию и поддержанию системного воспалительного ответа и окислительного стресса [29]. Наоборот, адипонектин является важным стимулятором NO-синтазы и дополнительно обеспечивает защиту от окислительного стресса и резистентности к инсулину. Снижение уровня циркулирующего адипонектина при ожирении связано с подавлением его синтеза провоспалительными адипокинами.
Все вышеперечисленные метаболические нарушения не только увеличивают риски развития ССЗ, но и, вызывая резистентность к инсулину, способствуют развитию СД 2-го типа. Следует отметить, что гиперинсулинемия и ИР при ожирении могут вызывать АГ посредством не только гиперстимуляции САС, но и через реализацию антинатрийуретического эффекта [30].
Есть и другие механизмы, посредством которых ожирение может способствовать развитию АГ. Например, апноэ сна — частое осложнение ожирения, может вызвать изменения в гипоталамо-гипофизарно-надпочечниковой системе, повышение уровня кортизола, а также дополнительную активацию СНС (рис. 1).
Вклад снижения веса в контроль уровня АГ
Краеугольным камнем лечения АГ у пациентов с избыточной массой тела или ожирением является непосредственно снижение веса. Не менее важную роль в коррекции уровня АД играет соблюдение низкосолевой диеты. Потеря веса снижает гиперактивацию РААС и СНС, а уменьшение объема висцерального жира позволяет снизить выраженность ИР, что дополнительно способствует натрийурезу. В настоящее время доказано, что уменьшение массы тела на 10-15% от исходной способствует повышению чувствительности к инсулину, улучшает показатели углеводного и липидного обмена, а также позволяет снизить уровень АД при его повышении [31, 32].
Основа мероприятий по коррекции массы тела — изменение образа жизни, повышение физической активности и изменение диеты с целью достижения баланса между потреблением и расходованием энергии. Наиболее эффективной и физиологичной следует считать диету со сниженным содержанием насыщенных жиров, повышением доли сложных углеводов, обеспечивающую умеренный дефицит калорийности в 500-600 кКал. Сочетание повышенной физической нагрузки с калорийными ограничениями приводит к более выраженному снижению веса и изменениям конфигурации тела (жир по сравнению с мышцами), чем только диета или только физическая активность [33]. При недостаточной эффективности немедикаментозных методов лечения или наличии определенных показаний возникает необходимость медикаментозной или даже хирургической коррекции веса тела, но эти мероприятия должны осуществляться только на фоне продолжающихся немедикаментозных вмешательств [34]. Показанием к применению лекарственных препаратов, снижающих вес, является ИМТ ≥30 кг/м2 или ≥27 кг/м2 в сочетании с абдоминальным ожирением, наследственной предрасположенностью к СД 2-го типа и наличием факторов риска сердечно-сосудистых осложнений (дислипидемия, АГ и СД 2-го типа).
Фармакотерапия помогает пациентам уменьшить связанные с ожирением риски для здоровья и улучшить качество жизни. Она также помогает предупредить развитие сопутствующих заболеваний, связанных с ожирением (например, АГ, СД 2-го типа). Определяя медикаментозную тактику лечения ожирения, следует помнить о высокой степени сердечно-сосудистого риска у больных с ожирением и учитывать влияние препаратов центрального действия [35].
Эффективность фармакотерапии следует оценивать через 3 мес. Если достигнуто удовлетворительное снижение массы тела (более 5% у лиц, не страдающих СД, и более 3% у лиц с СД), то лечение продолжают; в противном случае (отсутствие ответа на лечение) препараты отменяют [36, 37].
Считается, что на первых этапах вполне реально снизить вес на 5-10% от исходного, чтобы оценить положительное влияние потери веса на заболевания, связанные с ожирением. Снижение веса на 1 кг приводит к снижению САД на 1,1 мм рт. ст. (95% доверительный интервал (ДИ) 0,7-1,4) и ДАД — на 0,9 мм рт. ст. (95% ДИ 0,6-1,3) [38]. Уменьшение веса на 5 кг снижает уровень глюкозы у пациентов с СД на 1 ммоль/л, или на 18 мг%, что соответствует эффекту некоторых гипогликемических препаратов, при этом улучшение контроля над углеводным обменом не зависит от способа, которым оно было достигнуто [39].
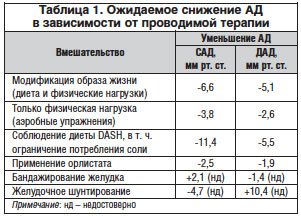
Эффективность модификации образа жизни в отношении снижения АД у пациентов с избыточной массой тела зависит от величины потери веса. Уменьшение всего на 2 кг посредством диеты может позволить, по данным исследований, снизить САД на 4 мм рт. ст. и ДАД — на 3 мм рт. ст. [40]. Метаанализ 25 рандомизированных исследований показал, что снижение веса на 5,1 кг, достигнутое ограничением калоража, повышением физической активности или сочетанием того и другого, может привести к снижению САД на 4,4 мм рт. ст. и ДАД — на 3,6 мм рт. ст. (табл. 1). Каждый 1 кг потери веса связан в среднем с уменьшением САД на 1 мм рт. ст. и ДАД — на 0,92 мм рт. ст. Потеря более 5 кг веса связана с более значимым снижением АД: САД в среднем снижается до 6,6 мм рт. ст., а ДАД — на 5,1 мм рт. ст. У пациентов с ожирением II степени (ИМТ 35-39,9 кг/м2) или III степени (ИМТ >40 кг/м2) уменьшение АД после снижения веса более чем на 10 кг еще сильнее выражено: САД уменьшается на 15 мм рт. ст., а ДАД — на 6 мм рт. ст. [41, 42].
Физическая нагрузка (аэробные упражнения) приводит к снижению уровня АД у пациентов как с повышенным АД, так и с его нормальным значением. Метаанализ 54 рандомизированных контролируемых исследований позволил сделать вывод, что аэробные упражнения могут снизить САД и ДАД на 3,8 и 2,6 мм рт. ст. соответственно, в то время как потеря веса составила всего 0,4 кг [43]. Тем не менее это указывает на то, что физические упражнения позволяют корректировать уровень АД независимо от снижения веса — вероятнее всего, за счет модулирования резистентности к инсулину и гиперинсулинемии.
Характер питания также оказывает благотворное влияние на снижение АД. Наиболее известна DASH-диета (Dietary Approaches to Stop Hypertension). После 8 нед. соблюдения диеты, богатой фруктами и овощами, обезжиренными молочными продуктами, с пониженным содержанием жиров САД и ДАД снизились на 11,4 и 5,5 мм рт. ст. соответственно у лиц с АГ по сравнению с контролем диеты [44]. При ограничении потребления соли от 3,5 до 1,2 г/сут и соблюдении диетических рекомендаций, согласно DASH, наблюдалось дальнейшее снижение САД на 7,1 мм рт. ст. у лиц без АГ и на 11,5 мм рт. ст. — у лиц с АГ [45].
Положительное действие снижения веса в лечении пациентов с АГ и другими ССЗ может заключаться также в том, что уменьшение количества внутрибрюшного жира ослабляет механическое сдавление почек, что может привести к улучшению их кровоснабжения и снижению активности РААС. Уменьшение жировой ткани внутри и вокруг почек может привести к снижению интерстициального давления, компрессии тонкой части петли Генле, увеличению кровотока в vasa recta, уменьшению канальцевой реабсорбции Na+ и воды [46]. Тем самым снижение веса, достигнутое как немедикаментозным, так и медикаментозным воздействием, может позволить скорректировать уровень АД.
Фармакотерапия ожирения и ее влияние на уровень АД
Медикаментозное лечение ожирения можно проводить только в дополнение к изменению образа жизни, если при этом не происходит необходимого снижения веса.
В настоящее время орлистат (оригинальный препарат Ксеникал®) является единственным препаратом, одобренным в качестве долгосрочной терапии ожирения. Орлистат тормозит всасывание жиров пищи в желудочно-кишечном тракте вследствие ингибирования желудочно-кишечных липаз — ключевых ферментов, участвующих в гидролизе триглицеридов пищи, высвобождении жирных кислот и моноглицеридов [47]. Это приводит к тому, что около 30% триглицеридов пищи не переваривается и не всасывается, что позволяет создать дополнительный дефицит калорий по сравнению с применением только гипокалорийной диеты.
В проспективном рандомизированном плацебо-контролируемом исследовании XENDOS (3304 пациента с ожирением) подтвердились эффективность и безопасность длительной терапии орлистатом (Ксеникал®) у больных ожирением: к концу 4-го года терапии уменьшение веса составило около 6 кг, а снижение САД и ДАД — 4,9 и 2,6 мм рт. ст. соответственно. У больных с ожирением и исходным ДАД более 90 мм рт. ст. к концу первого года терапии препаратом Ксеникал® ДАД уменьшилось на 7,9% [48]. Тем не менее дополнительный гипотензивный эффект орлистата по сравнению с плацебо довольно скромный: снижение САД только на 1,5 мм рт. ст. и ДАД — на 0,7 мм рт. ст. [49].
В Германии в исследовании 15 549 тучных пациентов с сопутствующими заболеваниями XXL (Xenical Large Study) среднее снижение массы тела составило 10,7%. Более 5% веса потеряли 87% пациентов, а 51% больных — более 10% от исходной массы тела на фоне терапии орлистатом на протяжении в среднем 7,1 мес. Снижение САД и ДАД в конце исследования составило 8,7 и 5,1 мм рт. ст. соответственно. У пациентов с АГ (их в исследовании был 41% от общего числа пациентов) в среднем САД снизилось на 12,9 мм рт. ст., а ДАД — на 7,6 мм рт. ст. [50].
Недавний метаанализ 4 исследований показал, что независимый от снижения веса гипотензивный эффект орлистата составляет -2,5 мм рт. ст. САД и -1,9 мм рт. ст. ДАД [51].
В российском исследовании препарата Ксеникал® у пациентов с АГ и метаболическим синдромом исходно средняя масса тела составила 111,5±5,4 кг, ИМТ — 36,9±1,3 кг/м2. До лечения средние показатели САД составляли 140,5±2,9 мм рт. ст., а средние значения ДАД — 90,0±2,1 мм рт. ст. Через 24 нед. терапии орлистатом на фоне снижения массы тела (105,0±3,2 кг) зарегистрировано достоверное снижение САД до 124,0±2,7 мм рт. ст. и ДАД — до 77,0±0,9 мм рт. ст. Гипотензивный эффект препарата сопровождался выраженным улучшением клинического состояния больных [52].
Результаты проведенного в России исследования препарата Ксеникал® показали высокую клиническую эффективность в отношении снижения массы тела у больных с ожирением. Через 12 нед. снижение массы тела на фоне применения препарата Ксеникал® было 5,26 кг, что составило 5,2% от исходной массы тела. Число пациентов, потерявших не менее 5% массы тела, было равно 51,2%, а не менее 10% массы тела — 5,9%. Среднее снижение САД уже после 12 нед. лечения составило 1,8 мм рт. ст., а ДАД — 3,0 мм рт. ст., что было статистически достоверным (p<0,0001) [53].
Заключение
Ожирение — это не только избыточный объем жировой ткани вследствие нарушения питания и недостаточного уровня физической активности, но и сложный комплекс гемодинамических и метаболических нарушений. Уменьшение массы тела у пациентов с ожирением сопровождается независимым снижением АД. В фармакотерапии ожирения, сочетающегося с АГ, коррекция веса является важным компонентом в общей схеме: даже умеренное уменьшение веса позволяет снизить АД и риск сердечно-сосудистых осложнений. На сегодняшний день наиболее безопасным препаратом для коррекции ожирения и длительной его терапии у пациентов с АГ является Ксеникал®.
Источник